soluții alcaline
Soluții aproximative. Cele mai frecvente alcalii in practica de laborator sunt soluții de NaOH hidroxid de sodiu. Soluțiile de hidroxid de potasiu KOH prepara rare ca soluții de amoniac sunt aproape întotdeauna gata să cumpere.
Hidroxid de sodiu (sau hidroxid de potasiu) este disponibil comercial în preparate: tehnice, pure sau chimic pură. Diferența dintre ele constă în procentul de NaOH (sau KOH) 1 și, prin urmare, impurități. * NaOH tehnic conține cantități semnificative de NaCl, Na2CO3, Na2SiO3, Fe2O3 și t. D. Reactivul pură conține o cantitate minimă de aceste impurități, ca chimic „reactiv din punct de vedere pur conține numai urme de ele.
sodă caustică tehnic vândut în butoaie din fontă, curat - bucăți de plăci și formă -sa chimic pură de bare sau granule.
Când dizolvat alcalin este o încălzire puternică, în special în acele locuri în care bucățile de minciuna ei. Pentru a dizolva mers mai repede, soluția trebuie să fie tot timpul sub agitare cu o baghetă de sticlă.
Aplicați un bol de sticlă prin dizolvarea alcaliei nu este recomandată, deoarece se poate rupe cu ușurință și rulează pot suferi ca o soluție concentrată de corozivă alcalin pentru piele, îmbrăcăminte și încălțăminte. Dacă trebuie să gătesc cantități mici de substanțe alcaline, este posibil să se dizolve într-un recipient de sticlă.
Bucăți de mâinile goale alcaline nu pot lua, acestea ar trebui să ia creuzete căpușă, pensete speciale, sau cel puțin mâinile, dar asigurați-vă că pentru a purta mănuși de cauciuc.
Inițial, recomandabil să se pregătească soluții concentrate de densitate alcaline 1,35-1,45 g / cm3, t. E. 40% pe 32 Configuratie. In astfel de soluții concentrate
* Tehnica este adesea numit sodă caustică sodă caustică.
alcaline multe impurități și nu se dizolvă în repaus soluția depozitată pe fund. Stabilindu soluție alcalină concentrat continuă timp de câteva zile (cel puțin două) *. Soluția de supernatant a fost decantat cu atenție, cel mai bun sifon, într-un alt vas, iar peleta aruncate sau consumate pentru spălat vase.
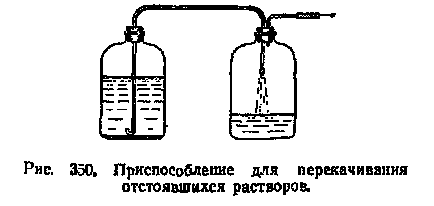
În cazul în care laboratorul de multe ori și în cantități mari, pentru a prepara o soluție alcalină, utilizați următoarea metodă. Mai întâi dizolvat complet alcalin într-un vas de porțelan, și atunci când soluția este răcită ușor (până la 40-50 ° C), se toarnă printr-o pâlnie într-un flacon de sticlă cu o capacitate adecvată. Sticla a fost închisă bine cu un dop de cauciuc, prevăzut cu o gaură în care este introdus un tub de clorură de calciu umplut cu sodă var (pentru a absorbi dioxidul de carbon). Când alcalii și soluționează în partea inferioară se formează stratul de sedimente brusc delimitat (1-2 cm din partea de jos), soluția stratul superior este turnat într-o altă sticlă. Dopul de cauciuc este inserat în ultimele două tuburi, unul dintre care trebuie să includă aproximativ 1/3 din înălțimea sticlei, iar celălalt ar trebui să fie de 1-2 cm sub tubul (Fig. 350).
La capătul exterior al unui tub de sticlă lung este împins tub de cauciuc, cu capătul de sticlă, care este coborât în alcalii sticla supernatant. Capătul inferior al tubului să fie îndoite așa cum este prezentat în Fig. 350. Acest lucru previne capăt de captare a nămolului de pe fundul sticlei, chiar dacă la sfârșitul atinge tub precipitat. tub scurt conectat la pompa de vid. Porniți pompa, soluția supernatantă este pompat rapid și sigur în cealaltă sticlă. alcalii transfuzionale trebuie să vă asigurați că tubul este coborât în vasul cu alcalii supernatant, neinvocate din sedimentul de jos. Prin urmare, este la începutul transfuziei menținut destul de mare deasupra precipitatului, reducând treptat la sfârșitul transfuzie.
* În mod natural, soluția de hidroxid de sodiu trebuie să stea fără a avea acces la acestea dioxid de carbon. soluții concentrate de alcalii puternice dezalcalizate sticle de sticlă, cu toate acestea vnutrennyayachast sticle trebuie să fie acoperite cu parafină sau un amestec de vaselină și cerizină ceară sau aliaj cu polietilenă (cm. Ch. 3, „Dopurile și manipulare“).
Pentru a acoperi peretele sticlei câteva parafină piesele sale sunt plasate în interiorul sticlei și ultimul este încălzit într-un cuptor sau peste un cuptor electric sau arzător cu gaz (cu atenție) până când 60-8O0C Când ceara topită, sticla este rotit și distribuie masa topită cu un strat subțire pe întreaga suprafață interioară.
Parafina sau strat cerezine poate fi aplicat prin aplicarea unei soluții a acestor substanțe în benzină de aviație. Parafina a fost dizolvat mai întâi în benzină, iar soluția rezultată se toarnă în sticlă, care trebuie să fie acoperită în parafină. Pereții sticlelor spălate introducerea parafinei soluție, încet transformându-l „pe axa în poziție orizontală. Când sticla se formează pelicula de ceară, sticla a fost purjat cu aer până când nu benzină. Apoi sticla clătite o dată sau de două ori cu vapori de apă. Numai după aceea poate fi umplută cu un metal alcalin sau alt lichid.
Prelucrarea pentru depozitarea sticlelor baze importante în special pentru laboratoarele analitice, deoarece previne contaminarea produselor soluții de sticlă titrate de levigare.
Soluție Titer tickle (m. E. Concentrația exactă a soluției) este cel mai bine instalat la o soluție de acid oxalic (C2H2O4 • 2H2O) *.
Vânzarea acid oxalic trebuie dată sau de două ori recristalizată și numai după aceea folosită pentru soluția exactă preparare. Este diacid și, prin urmare, greutatea sa echivalentă este jumătate din molecular. Deoarece acesta din urmă este egală cu 126.0665, greutatea echivalentă a voinței ei:
La prepararea și 0,1. soluție de NaOH, trebuie să avem o soluție de acid oxalic este aceeași normalitate, la care 1 l de soluție este necesar să se ia:
Dar acest număr nu este necesar să instalați titrul soluție; suficientă pentru a prepara 100 ml sau 250 ml maxim. În acest scop, pe o balanță analitică cântărește aproximativ 0,63 grame (până la 100 ml) a fost recristalizat acid oxalic cu o precizie la a patra zecimală.
Începând de la o captura Porțiile de testare a lucrătorilor pentru a instala titru încearcă adesea să cântărească specificat cu precizie în manualul de utilizare cantitatea de substanță (în acest caz 0.6303 g). Pentru a face acest lucru, în orice caz, nu este necesar, așa cum este în mod inevitabil, necesită mai multe cântărire Rudă
* Deoarece hidroxidul de sodiu absoarbe ușor dioxidul de carbon, alcali întotdeauna este prezent carbonatul de sodiu. Prin urmare, prepararea unei soluții de hidroxid de sodiu, este necesar să se stabilească concentrația acesteia prin titrare loturi precise de soluții de acizi organici cum ar fi acidul oxalic, malic, etc., nu este necesară pentru a dilua soluția concentrată într-un balon gradat de adaptare exact nivelului soluției până la marcaj .; Puteți, se toarnă în sticlă, în cazul în care acesta va fi stocat, se adaugă apă cu un cilindru gradat. Se va aprecia că în prepararea soluțiilor de atenție alcaline caustice trebuie acordată pentru a proteja soluțiile de aer de dioxid de carbon. Toate operațiunile de reducere, în care soluția poate veni în contact cu aerul, este foarte de dorit și de rulare în substanțe dosypany în containere. Ca urmare a materialului devine pe platanul de cântărire și pe peretele exterior al recipientului și cântărit cu precizie cantitatea de substanță nu poate fi complet transferat în balonul volumetric. Prin urmare, soluția preparată va fi inexacte. În cele din urmă, multe substanțe în aer variază (sau pierde apa de cristalizare se spune că „erodeze“, absorb dioxidul de carbon din aer, și așa mai departe. D.). Prin urmare, cu cât cântăririi; cu atât mai mare posibilitatea contaminării substanței. Prin urmare, primul care ia o mostră de solzi technochemical, convergente> schuyusya cu necesară în primele două zecimale, iar apoi se determină pe o masă precisă balanță analitică. O porțiune a fost dizolvată într-un volum corespunzător de solvent.
Cunoscând masa substanței luate și volumul de soluție este ușor pentru a calcula concentrația exactă, care, în cazul nostru nu este egal cu 0,1N. un pic mai puțin. Cu această metodă de calcul este oarecum complicat, dar precizie îmbunătățită și economii semnificative de timp.
Atunci când soluția este gata, este luat din pipeta 20 ml, se transferă într-un balon conic, se adaugă câteva picături de fenolftaleină și se titrează cu soluția alcalină preparată până la o culoare roz ușoară.
Exemplu. La titrarea soluției alcaline consumate 22,05 ml Se calculează normalitatea și titrul său.
Acidul oxalic a fost luată în loc de 0.6223 g din suma calculată teoretic de 0.6303 Prin urmare, concentrația soluției sale nu este tocmai 0,1N. și egal
Pentru a calcula normalitatea alcalină a soluției, ar trebui să utilizeze relația N [Vi = / V2-V2, t. E. Produsul din volumul unui cunoscut volum soluție normalitatea egală cu produsul de normalitate soluție necunoscută. În cazul nostru, este o soluție de acid oxalic, prin urmare
Normalitatea soluției alcaline este 0.08955.
În cazurile în care este necesar soluția purificată de înaltă hidroxid de sodiu, sau ele sunt preparate din soluții alcoolice de NaOH sau amalgam de sodiu.
sodiu metalic se dizolvă în alcool etilic deshidratat posibil. Soluția de alcool este preparată cu aproximativ 5%. mici de sticlă umplute la jumătate și nu mai mult de 3U volumul său cu petrol lampant sau nafta curate, tarate tehno-chimice vesgGh fracție sau greutăți mici. Dintre băncile care stochează sodiu metalic sub gaz lampant sau nafta, luați forceps sau bucăți de sodiu cuțit și de tăiere a cuțitului coaja exterior, transferat într-un pahar tarată, cântărind cantitatea dorită. În această operațiune, greutatea și recipientul este pus pe platanul din stânga, și sticlă cu kerosen - cupa dreapta. *
Uneori, în loc este utilizat sodiu metalic sau de metal de potasiu dizolvat în alcool cu hidroxid de sodiu sau hidroxid de potasiu. Trebuie reamintit faptul că solubilitatea la 28 ° C în etanol NaOH mai mică decât solubilitatea KOH, aproape de două ori (respectiv 14,7 g / 100 g și 27,9 g / 100 g).
soluții alcaline alcoolice au de obicei slabozheltuyu osmolepiem colorare cauzată de acțiunea alcaliilor asupra impurităților, în special compuși nesaturați care pot fi prezenți în alcool.
Pentru prepararea soluțiilor de KOH incolore, fără îngălbenire și întunecare utilizării și depozitării, se recomandă următoarea metodă. Aproximativ 5 ml Bu tilata de aluminiu se adaugă, sub agitare, la 1 litru de etanol la o temperatură de aproximativ 20 ° C. Acest amestec a fost lăsat să stea timp de câteva săptămâni, dar nu mai puțin de o lună, și apoi se toarnă cu atenție alcool (de preferință cu ajutorul unui sifon decantează) și adăugat la aceasta cantitatea necesară de KOH. butoxidul de aluminiu provoacă precipitarea toate impuritățile care afectează îngălbenirea sau întunecarea soluții alcoolice de baze.
Pentru o soluție de NaOH se poate utiliza, de asemenea amalgam de sodiu. Pentru prepararea ei se cîntăresc 2,5 g de sodiu metalic și 100 g de mercur. Mercurul este turnat în tub, acesta este plasat într-un pahar, a pus într-o ceașcă de porțelan. Înainte de recoltare baghetă de sticlă de mai multe trase din capătul (tije de lungime 35-40 cm). Pe un băț pus pe o bucată de azbest, astfel încât atunci când coborârea tubului tija este azbestul închis. In aceasta bagheta shemoschi este îndepărtată din bucata de parafină sodiu metalic mazăre de dimensiuni, a șters repede cu hârtie de filtru și aplicat la mercur. Rețineți că, în acest caz, capacitatea de a lumineze intermitent cu ușurință. Treptat, mercurul este introdus în întregul sodiu metalic. Amalgamul (mercur metalic în soluție) trebuie să fie în stare lichidă, dar se poate solidifica treptat. Amalgamul lichid este turnat într-un recipient de apă, eliberat anterior de dioxid de carbon. Nava trebuie prevăzută cu tubul de evacuare cu o supapă Bunsen. Dacă amalgamul sa întărit, tubul trebuie să fie rupte și bucăți de amalgam plasate în apă care nu conține dioxid de carbon. După două zile de soluție de hidroxid de sodiu a fost decantată din mercur și normalitatea sa este stabilită așa cum este descris mai sus.
La prepararea soluțiilor, titrul care este stabilit de analit, cm. Mai sus.
Pentru a prepara soluțiile exacte de baze se utilizează ca metodă de schimb ionic. rășini schimbătoare de anioni poate fi utilizată pentru purificarea soluțiilor de hidroxid de sodiu și hidroxid de potasiu și carbonații prepararea soluțiilor precise de hidroxid de sodiu și hidroxid de potasiu, în baza șarjele exacte de clorură de sodiu sau clorură de potasiu.
Dacă este necesar doar pentru a separa carbonații contaminante și ionii de clor dizolvat, prima porțiune care trece prin coloană în formă de CI-soluție este eliminată atât timp cât ionul clorură nu mai detectabil în soluția de probă este.
Saturate ionii de carbonat de schimbătoare de anioni poate fi transformat din nou într-o formă C1-metoda uzuală, adică. E. O coloană de acid clorhidric, apoi coloana a fost spălată bine cu apă.
Pentru a obține o soluție corectă „de hidroxid de sodiu sau hidroxid de potasiu probă calculat de clorură de sodiu sau clorură de potasiu, cântărit pe o balanță analitică și se dizolvă în apă distilată sau demineralizată și soluția rezultată a fost trecută printr-o coloană chro-matograficheskuyu umplute Anio-niți în formă OH. Din coloana va urmări concentrația calculată a soluției alcaline.
Soluții exacte de NaOH sau KOH este cel mai bine păstrat într-un recipient de polietilenă, în care substanța alcalină nu funcționează, sau într-un pahar în interiorul unui cerată.